SÍNTESE DE a-SULFINIL ENONAS
Francisco Carlos Biaggio a (PQ), Reinaldo Romero Vargas b (P.Q.),
Blanka Wladislaw c (P.Q.), Liliana Marzorati c (P.Q.)
Palavras-chave: Alquilação, b-Cetossulfóxidos, a-Sulfinil Enonas.
Introdução: A utilização do grupo sulfinila na síntese de compostos biologicamente ativos tem sido extensamente estudada nas últimas décadas1. Dentre estes sulfinil derivados, destacam-se as a-sulfinil enonas 1, na síntese de componentes de feromônio de insetos2, entre outros exemplos. Atualmente este tipo de substrato tem sido usado em reações de Diels-Alder ou como aceptores ativados de Michael. Estes precursores são obtidos a partir de complexas rotas sintéticas3.
Objetivos: Este trabalho tem como objetivo desenvolver uma metodologia de obtenção de a-sulfinil enonas 1, a partir de b-cetossulfóxidos, estudando as possíveis variáveis reacionais, buscando o melhor rendimento para cada etapa.
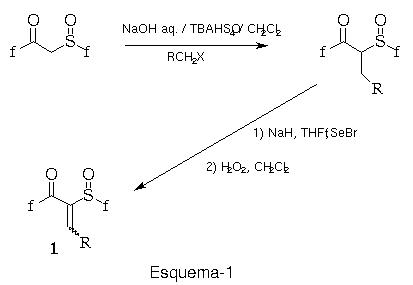
Metodologia: A obtenção das a-sulfinil enonas 1, envolve duas etapas: a) alquilação dos b-ceto-sulfóxidos realizada em condições de catálise de transferência de fase (c.t.f.), b) selenização e posterior oxidação do alquil b-cetossulfóxido, conforme mostrado no Esquema-1.
Resultados: Clement4 estudou a alquilação de b-cetossulfóxidos em condições de catálise de transferência de fase (c.t.f.), mas no entanto, os produtos obtidos C-alquilado e/ou O-alquilado dependiam do alquilante usado. A alquilação de b-cetossulfóxidos em meio homogêneo5, usando hidreto de sódio como base, forneceu bons rendimentos para metil derivados, no entanto, os derivados etilados e benzilados forneceram baixos rendimentos. Alquilações no carbono, usando haletos de alquila secundários, não foram observadas6. Os b-cetossulfóxidos foram por nós alquilados em condições de c.t.f., e os resultados foram coerentes com os observados por Clement. Estudos de selenização de compostos carbonílicos com haletos de fenilselenila e posterior oxidação, geraram compostos carbonílicos a,b-insaturados em ótimos rendimentos7. A selenização por nós realizada foi conduzida em meio homogêneo, com hidreto de sódio como base. Após extração, o óleo obtido foi oxidado com H2O2, a 0oC sob forte agitação. Os resultados destas reações encontram-se na Tabela-1 e são referentes aos produtos isolados. Cabe ressaltar que quando a selenização foi realizada como primeira etapa, a alquilação mesmo com iodeto de metila não foi observada para as mesmas condições. Isto deve-se provavelmente ao grande volume do grupo fenilselenila já presente na molécula.

Tabela-1: Obtenção de a-sulfinil enonas 1 a partir de b-cetossulfóxidos.
|
R |
h (%) alquilação |
h (%) selen. / oxid. |
|
H |
90 |
65 |
|
CH3 |
70 |
45 |
|
f |
63 |
51 |
Conclusões: A alquilação de b-cetossulfóxidos possui a limitação com relação ao alquilante usado e merece um estudo mais detalhado sobre esta variável. No geral, a obtenção de a-sulfinil enonas mostrou-se perfeitamente viável a partir de b-cetossulfóxidos. Isto nos dá a confirmação de que se partirmos de substratos quirais, preparados a partir de metil p-tolil sulfóxido quiral8, obteremos as a-sulfinil enonas quirais.
Carreño, M.C.; Chem. Rev. 1995, 95, 1717.
Hayes, P.; Maignan, C.; Synthesis 1999, 783.
Hayes, P.; Maignan, C.; Tetrahedron: Asymmetry 1999, 10, 1041.
Clement, B; Chemiker-Zeitung 1980, 104, 368.
Russell, G.A.; Mikol, G.J.; J.Am. Chem. Soc. 1966, 88, 5498.
Gassman, P.G.; Richmond, G.D.; J. Org. Chem. 1966, 31, 2355.
Reich, H.J.; Reich, I.L.; Renga, J.M.; J. Am. Chem. Soc. 1973, 95, 5813.
Kunieda, N.; Nokami, Y.; Kinoshita, M.; Chem. Lett. 1974, 369.