ESTUDOS
COMPARATIVOS DA REDUÇÃO CATÓDICA DO Mo(VI) EM
ELETRODOS DE MERCÚRIO E CARBONO VÍTREO
Denise Lowinsohn (IC), Luis Kosminsky (PG) e Mauro Bertotti (PQ)
Instituto de Química - USP, São Paulo, SP, Brasil
Palavras-chave:
molibdênio, eletrodo de mercúrio, eletrodo de
carbono vítreo
Introdução
Estudos
eletroquímicos sobre a redução polarográfica
do Mo(VI) utilizando-se eletrodo gotejante de mercúrio(EGHg)
em diferentes condições experimentais são
largamente encontrados na literatura[1]. Todavia, em
eletrodo pendente de mercúrio e eletrodo de carbono vítreo
existem menos referências sobre este processo eletroquímico.
Desta maneira, é de extrema relevância comparar o
comportamento eletroquímico do Mo(VI) em diferentes tipos de
eletrodo (mercúrio gotejante/ pendente e carbono vítreo)
para melhor explicar a redução do Mo(VI), influenciada
pela natureza do eletrodos. A caracterização das
espécies de Mo(VI) geradas durante a acidificação
constitui-se em tarefa díficil devido à complexidade da
química do molibdênio, rica em processos de
polimerização. Desta forma, o comportamento
eletroquímico do Mo(VI) é relativamente complicado
devido à presença de diferentes espécies em
solução.
Neste
contexto, o presente trabalho destaca alguns resultados relacionados
a estudos sobre a redução catódica do Mo(VI) em
H2SO4 0,1M e 1mM nos diferentes tipos de
eletrodos.
Parte
experimental
Reagentes:Todas
as soluções utilizadas nos experimentos foram
preparadas a partir de reagentes de pureza analítica
dissolvidos em água desionizada ou pela diluição
de ácidos concentrados comerciais. Para a eliminação
do oxigênio presente nas soluções, borbulhou-se
por cinco minutos o gás argônio previamente à
realização dos experimentos.
Instrumentação:
Na aquisição dos polarogramas foi empregado
potenciostato Polaroprocesseur (Tacussel), controlado por software
desenvolvido pela própria empresa. Os experimentos foram
realizados em célula eletroquímica convencional e
sistema de 3 eletrodos: gotejante ou pendente de mercúrio e
carbono vítreo (eletrodo de trabalho), platina (eletrodo
auxiliar) e Ag/AgCl, NaCl saturado (eletrodo de referência).
Eletrodo
de mercúrio: Os estudos envolvendo o uso do eletrodo
gotejante e pendente de mercúrio foram realizados em
célula Tacussel EGM200T, na qual pode–se trabalhar com
diferentes tempos de gotejamento e tamanhos da gota.
Eletrodo
de carbono vítreo: Foi empregado um eletrodo da
Bioanalytical Systems na forma de disco de carbono vítreo de 3
mm de diâmetro encapsulado em peça cilíndrica de
teflon.
Resultados e
discussões
O
voltamograma de solução de Mo(VI) 1mM em H2SO4
0,1M em eletrodo estático de mercúrio não
apresenta sinal de corrente até –0,05V, diferentemente do
que se observa ao se trabalhar com eletrodo gotejante de mercúrio.
Tal fato deve-se possivelmente à formação de
material adsorvido na superfície do eletrodo estático,
cuja influência é menos significativa ao se trabalhar
com eletrodo de área continua-mente renovada como o eletrodo
gotejante de mercúrio.
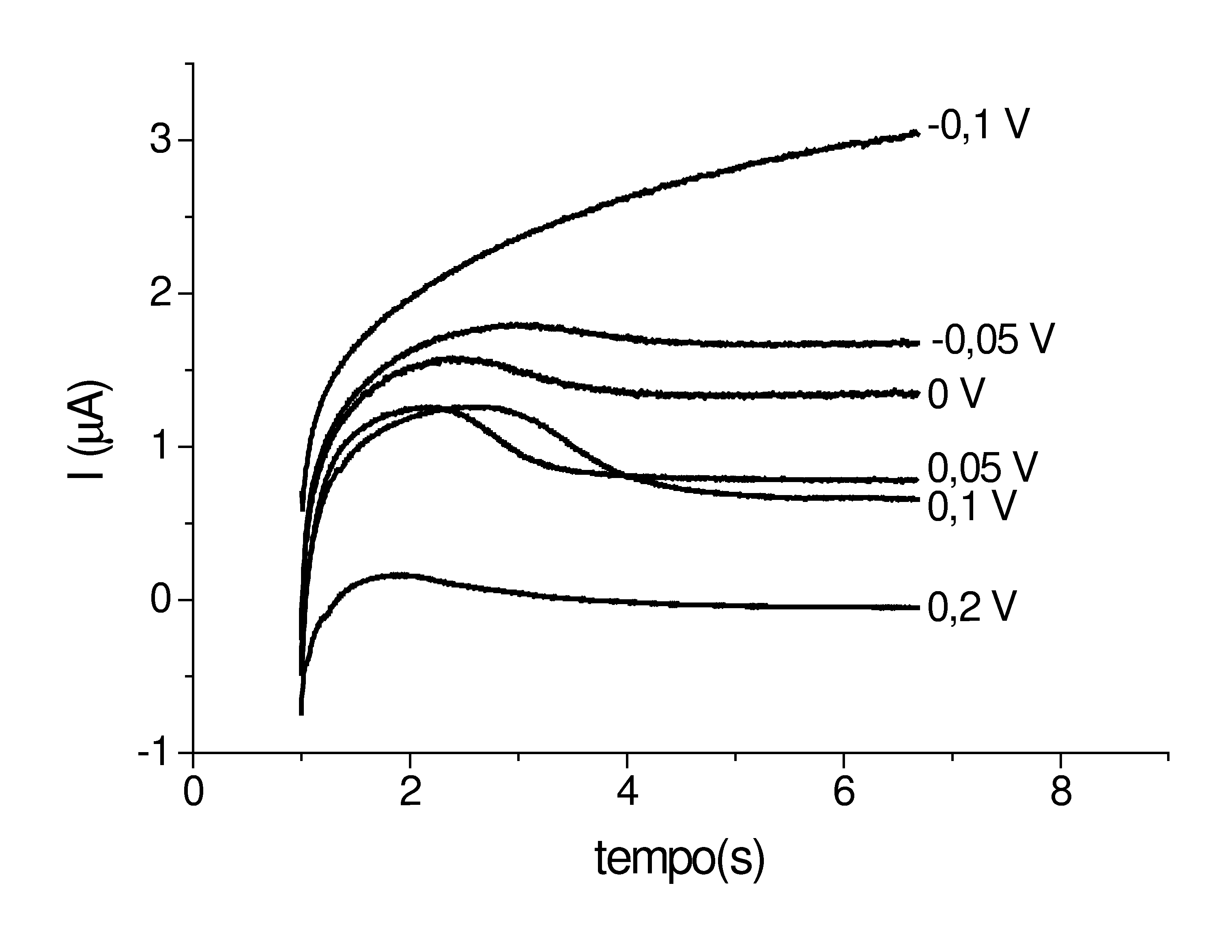
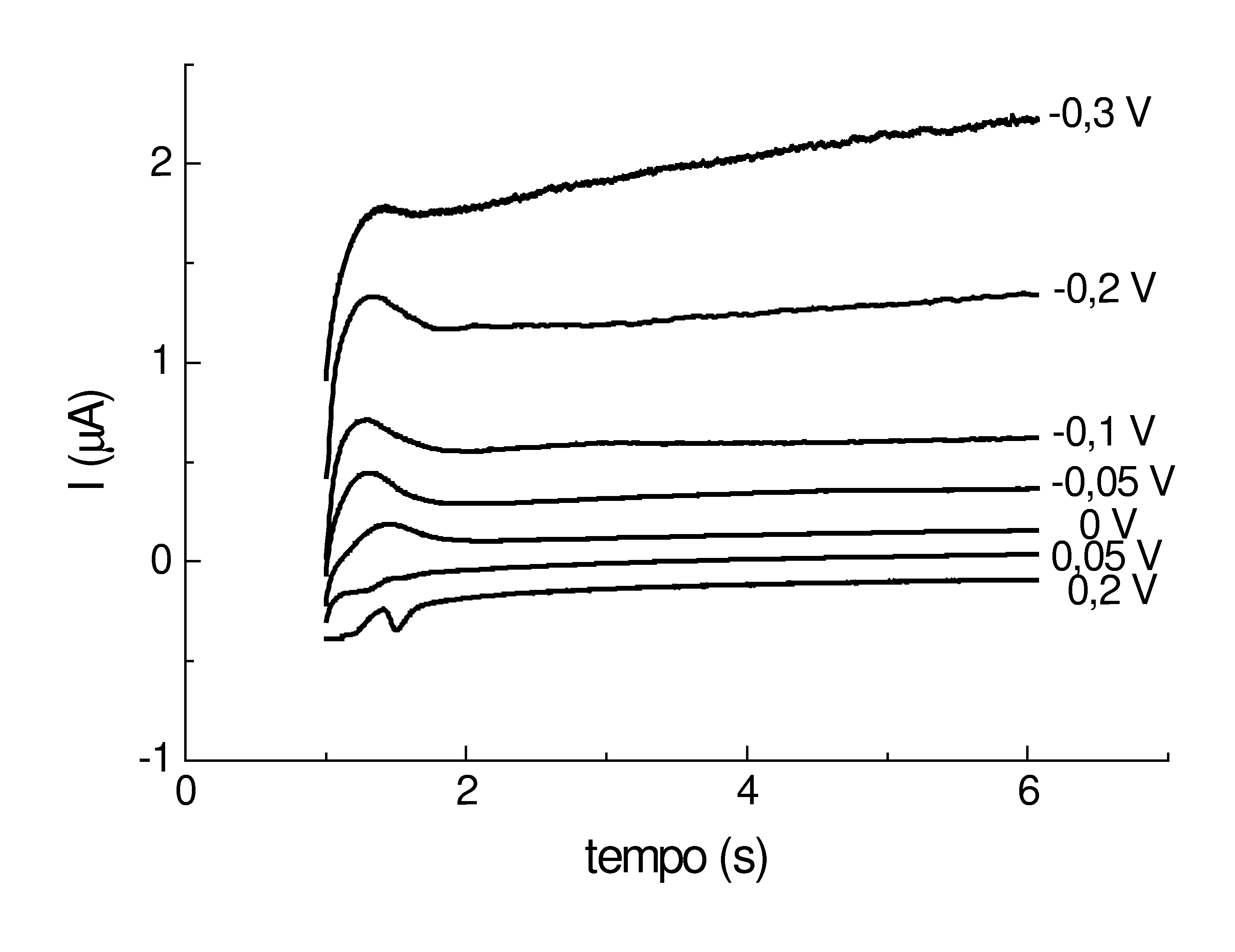
Com
base em estudos cronoamperométricos pode–se dizer que
ocorre adsorção do produto da redução do
Mo(VI) no mercúrio em potenciais menos nega-tivos. Este
processo de adsorção é favorecido em meio menos
ácido (figuras 1 e 2), ampliando a faixa de potencial em que
ocorre a imobilização na superfície do eletrodo.
Essas interações dependem do pH e podem ser explicadas
pela existência de diferentes formas de Mo(VI) ao se variar o
pH das soluções.
Fig.
1 – Cronoamperogramas de solução de Mo(VI) 1mM
Fig. 2 – Cronoamperogramas de solução de
Mo(VI) 1mM
em
H2SO4 0,1M. Eletrodo pendente de mercúrio.
em H2SO4 1mM. Eletrodo
pendente de mercúrio.
Nos
estudos procedidos com eletrodo de carbono vítreo observou-se
que a espécie de Mo(VI) presente em H2SO4
0,1M não é eletroativa, diferentemente do que
ocorre em H2SO4 1mM. Este fato é
concordante com trabalhos já publicados nos quais demonstra-se
a possibilidade de imobilização de filme de óxidos
de molibdênio em eletrodos de carbono vítreo em pH na
faixa de 2 a 3[2].
Portanto
as diferenças de comportamento eletroquímico do Mo(VI)
em eletrodo de mercúrio e em eletrodo de carbono vítreo
por serem significativas indicam que devem existir interações
químicas entre o molibdênio e o mercúrio,
favorecendo sua redução. Pretende-se explorar a
possibilidade de pré-concentração de Mo(VI) em
superfícies de mercúrio para o desenvolvimento de
método analítico.
Bibliografia
M.
Bertotti and R. Tokoro, J. Electroanal. Chem., 360
(1993) 39-54.
L.
Kosminsky and M. Bertotti, Electroanalysis, 11 (1999)
623-626.
FAPESP

