TITULAÇÕES POTENCIOMÉTRICAS de L-DOPA
com Gd3+ e Zn2+.
Ana Lucia Ramalho Mercê (PQ), Berta Covelo Rodríguez (PG), Eduardo Tatsuya Ferreira Kato (IC), Thereza Julyana Simião Denes (IC) .
Departamento de Química - Universidade Federal do Paraná.
anamerce@quimica.ufpr.br
palavras-chave: L-Dopa, complexos metálicos, titulação potenciométrica.
Introdução.
A doença de Parkinson é um dos distúrbios do movimento que mais acomete a população idosa. É uma doença degenerativa dos gânglios da base que causa tremor em repouso, rigidez muscular e hipocinesia. Freqüentemente idiopática, porém vários mecanismos implicados na gênese da degeneração neuronal têm sido objeto de interesse: ação de neurotoxinas ambientais, produção de radicais livres, anormalidades mitocondriais e envelhecimento cerebral. Atualmente, a levodopa (L-Dopa ou 3,4-dihidroxifenilalanina) é utilizada no tratamento do mal de parkinson por ser precursora da dopamina. A deficiência dessa substância no cérebro é responsável pela sintomatologia da doença. A eficácia terapêutica da levodopa, no início do tratamento, demonstra que 80% dos pacientes mostram melhora, sobretudo da rigidez e hipocinesia, e cerca de 20% retomam a função motora normal. Porém, com a progressão natural da doença, essa terapêutica perde sua eficácia gradativamente. Alguns dos efeitos colaterais são minimizados com a administração de outras drogas, concomitantemente com a L-Dopa, a fim de que a espectativa de vida dos indivíduos parkinsonianos seja melhorada(1-3).
A modelagem molecular tem sido uma das ferramentas usadas na interpretação dos resultados experimentais, relacionando estrutura molecular e propriedades eletrônicas com a estabilidade e reatividade dos sistemas moleculares, sendo o Zn 2+ um modelo metálico importante (4).
Objetivos.
Observação do comportamento da L-Dopa frente à complexação com os íons Zn2+ e Gd3+ para bioensaios na otimização da levodopaterapia. Neste estudo a modelagem molecular tem como objetivo verificar a viabilidade energética e conformacional da formação desses complexos metálicos, avaliados pela titulação potenciométrica.
Métodos.
Soluções
aquosas de L-Dopa na ausência e presença dos íons
metálicos Zn2+ e Gd3+ foram tituladas em
uma célula termostatizada(25,0
![]() 0,1 oC), em atmosfera inerte, com força iônica
constante. Pela adição de volumes conhecidos de base
padronizada aos sistemas obteve-se os valores de p[H]. Os programas
de computador BEST7 e SPE forneceram as constantes de estabilidade e
a distribuição das espécies presentes no
equilíbrio, respectivamente.
0,1 oC), em atmosfera inerte, com força iônica
constante. Pela adição de volumes conhecidos de base
padronizada aos sistemas obteve-se os valores de p[H]. Os programas
de computador BEST7 e SPE forneceram as constantes de estabilidade e
a distribuição das espécies presentes no
equilíbrio, respectivamente.
As análises conformacionais realizadas nos complexos L-Dopa:Zn2+, foram feitas por mecânica molecular utilizando-se os programas ChemDraw-Pro 3.5 e Chem3D-Pro 3.5 - CambridgeSoft Corporation, através do método semi-empírico MM2, minimização de energia.
Resultados e Discussão.
Figura 1 - Complexos possíveis de L-Dopa com Zn 2+.
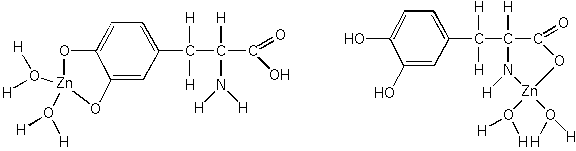
Os
cálculos de modelagem molecular, resultaram nos seguintes
valores de energia estérica, 21,99 Kcal/mol para a complexação
da L-Dopa com zinco (II) ligando-se ao sítio básico do
grupo fenólico e 28,17 Kcal/mol para a complexação
da L-Dopa com Zn2+ ligando-se com os sítios
básicos dos grupos aminocarboxílicos, já para o
comprimento das ligações foram obtidos resultados de
1,804 A, e, para os ângulos entre as ligações
obteve-se 112,16º. A constante de formação do
complexo L-Dopa (L) e Zn2+ (M) encontrada foi log K=12,83
![]() 0,01, com formação máxima a p[H] 7,2, para a
espécie ML. Para o complexo de Gd3+ (M) e L- Dopa
(L), as constantes de formação são log K1
=13,3
0,01, com formação máxima a p[H] 7,2, para a
espécie ML. Para o complexo de Gd3+ (M) e L- Dopa
(L), as constantes de formação são log K1
=13,3
![]() 0,4, para ML, e log K2=12,0
0,4, para ML, e log K2=12,0
![]() 0,4,
para ML2, com formações máximas em
p[H] 6,0 e 8,5 respectivamente.
0,4,
para ML2, com formações máximas em
p[H] 6,0 e 8,5 respectivamente.
A complexação da L-Dopa com o zinco é provavelmente mais estável quando a complexação ocorre com o grupo fenólico devido à menor energia estérica e menores tensões entre as ligações.
Referências Bibliográficas
1 - Stephen M. S., Essential Psychopharmacology, ed. Baltimore-Williams & Wilkins, San Diego -1996.
2 - Stone, T. W., Neuropharmacology, ed. Oxford University press, NY, 1995.
3 - Meneses, Murilo S.; Teive, Hélio A. G., Doença de Parkinson, ed. Guanabara Koogan, RJ,1996.
4 - User’s guide, CS Chem3D Pro / User’s guide, CS ChemDraw Pro,
Cambridge, 1995.