André Mauricio de Oliveira (PG), Claudio Luis Donnici (PQ),
Carlos Alberto Montanari (PQ)
Núcleo de Estudos em Química Medicinal (NEQUIM),
Departamento de Química, Instituto de Ciências Exatas,
Universidade Federal de Minas Gerais
Introdução: A atividade antiprotozoária das bisamidinas aromáticas é bem conhecida. Desde a década de 30 novos derivados têm sido testados, e atualmente seu espectro de atividade inclui: Acanthamoeba, Babesia canis, Crithidia fasciculata, Cryptosporium parvum, Giardia lambia, Leishmania sp., Plasmodium sp., Toxoplasma gondiie e Trypanossoma sp.. O uso das bisamidinas aromáticas contra a pneumonia causada por Pneumocystis carinii (PCP) remonta a 1958 com a pentamidina e a estilbamidina. Vários efeitos colaterais, contudo, seguem a administração da pentamidina e alguns de seus análogos. Além de apresentarem atividade variada, estes compostos encontram-se protonados em pH fisiológico, o que dificulta a determinação do seu modo de ação. Entretanto, existem diversas propostas, dentre as quais, a inibição no metabolismo e/ou síntese de ácidos nucléicos. Foi determinado que as bisamidinas aromáticas têm grande afinidade por seqüências do DNA ricas em bases AT, e este comportamento já foi verificado pela estrutura de raio X do complexo pentamidina - dodecâmero d(CGCGAATTCGCG)2. A pentamidina é uma molécula flexível, e na fenda menor do B-DNA adota uma conformação denominada isoélica, acompanhando a curvatura da fenda, com um vetor de comprimento igual a 9,13 Å, bastante próximo da distância equivalente a duas unidades de repetição de 4,61 Å, necessárias para produzir esta conformação. O trabalho desenvolvido por Montanari e colaboradores mostrou ser a estrutura isoélica aquela adotada pelas bisamidinas aromáticas na interação com esta seqüência.
Estudos prévios de Modelagem Molecular e QSAR onde os complexos entre diversos derivados bisamidínicos e o dodecâmero do DNA foram submetidos a um processo de busca conformacional no qual a energia de interação era calculada mostraram que derivados bisamidínicos heterocíclicos análogos à furamidina, particularmente os derivados isoxazólicos e 1,2,4-oxadiazólicos, apresentavam maior afinidade pela fenda menor do DNA (a energia de interação calculada é da ordem de –70 kcal/mol).
Objetivos: Estudar a síntese de compostos bisamidínicos heterocíclicos, do tipo isoxazólicos e 1,2,4-oxadiazólicos, propostos por planejamento racional por QSAR e Modelagem Molecular.

Resultados e Discussão:
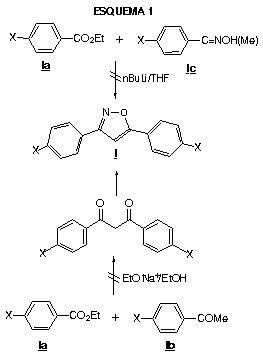
Inicialmente tentamos a síntese de derivados isoxazólicos 3,5-bis-para-fenilsubstituidos I (Esquema 1) a partir da condensação clássica entre o éster benzóico Ia e a acetofenona Ib correspondentes em meio etóxido de sódio/etanol seguida da ciclização por hidroxilamina, no entanto a necessária presença de grupos eletrón-retiradores em para impediu a condensação. Este efeito eletrônico também foi responsável pelo insucesso de outro método de ciclização a partir da condensação entre a oxima da acetofenona para-substituida Ic e o éster benzóico correspondente Ia com n-butil-lítio em THF anidro. Partimos então para a síntese dos 1,2,4-oxadiazóis propostos.
A
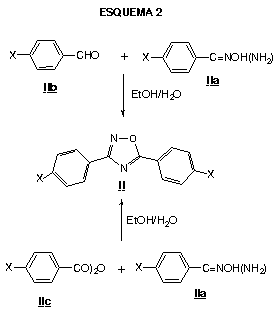
preparação da 4-(3-fenil-1,2,4-oxadiazol-5-il)
fenilamina (II) foi feita a partir de adaptação
do método proposto por Srivastava (Esquema 2): a
4-aminobenzamidoxima (IIa) obtida a partir da
reação de 4-aminobenzonitrila com cloridrato de
hidroxilamina e carbonato de sódio foi submetida à
reação com o benzaldeído (IIb)
redestilado (1:5 mol/mol) à temperatura ambiente
durante 5 dias; obteve-se após recristalização
do produto (etanol/água) um sólido laranja (P.F=
159-164 oC), rendimento de 38%. A identificação
espectroscópica por espectrometria na região do IV
caracterizou o heterocíclico 1,2,4-oxadiazólico:
IV (KBr,cm-1) 3300 (estir. NH2), 1450 (estir.
CN), 900 e 1050 (características do anel 1,2,4-oxadiazólico),
750 (CH anel 1,2,4-oxadiazólico), bem como os dados de
RMN de 1H e de 13C. No entanto, visando-se
aumento no rendimento para a preparação dos outros
1,2,4-oxadiazóis necessários estamos otimizando o
método de Tiemann (Esquema 2) que emprega a condensação,
em etanol aquoso, do anidrido carboxílico (IIc)
e da amidoxima (IIa) correspondentes, que devem ser
preparados.
CNPq, FAPEMIG, FINEP, PADCT